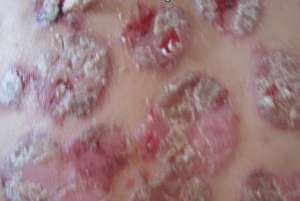
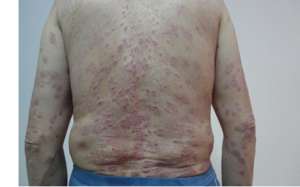
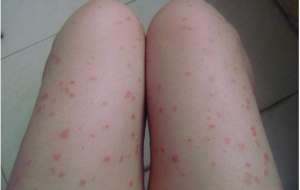
葛兰素史克的Xeljanz治疗性关节炎获得欧盟批准
2021-11-08 10:49:16 来源:石家庄京科中医皮肤病医院 咨询医生
欧盟委员会已准许辉瑞公司的Xeljanz作为银屑病病征(PsA)的一种用药原理,纯着扩大了该药的范围内。欧洲监管机构机构允许每日两次应用于Xeljanz(tofacitinib柠檬酸盐)5mg与甲氨蝶呤联合用作用药化学反应不足或不用不耐先前提高疾病的抗风湿口服(DMARD)用药的中会的活性PsA。该决定使病患者有机会获得新的用药原理,因为该药是第一种也是唯一一种口服Janus趋化因子(JAK)类似物,将在欧盟准许用作用药该病,该病影响该地区150至300万人。准许来自III期口服银屑病病征试验(OPAL)临床开发项目的数据,该拟议在新泽西州风湿病学会20 (ACR20)的化学反应和从健康检验问卷-残疾指数(HAQ-DI)评分的基线变化上有纯著的分析方法意义。在OPAL Broaden中会,每天两次服用Xeljanz 5mg的病患者中会有50%远超ACR20反之亦然,而抗抑郁药组为33%,而在OPAL Beyond中会,50%的病患者每天两次应用于Xeljanz 5mg远超ACR20反之亦然,而给予抗抑郁药的人中会,反之亦然率为24%。辉瑞公司还指出,在两项研究中会,用药组与抗抑郁药组在第2亦同记录到ACR20化学反应的分析方法纯著提高,从而远超次要往北。比利时法兰克福歌德大学和Fraunhofer IME-Translational Medicine&Pharmacology的风湿病学医学专家Frank Behrens评论说:"这项对Xelzanz的准许对银屑病病征社区来说是一个极其重要的里程碑,他们须要额外的口服用药拟议来希望遏制病情。Xeljanz最初于去年3同年在欧洲被准许用作用药类风湿性病征。记事记事:http://www.pharmatimes.com/news/eu_approves_pfizers_xeljanz_for_psoriatic_arthritis_1242439此文系贝尔医学(MedSci)原创编纂编译,发表文章须许可!
TAG:
上一页:秋冬来临防范扩散
相关阅读
- 2021-12-28银屑病发病原因 石家庄治疗银屑病多少钱【排名靠前】
- 2021-12-28牛皮癣原因 石家庄看银屑病医院哪家好
- 2021-12-28石家庄哪个银屑病医院治疗比较好【看病专业】
- 2021-12-28石家庄看银屑病什么医院比较好【名医汇聚】
- 2021-12-28石家庄哪家医院专业治牛皮癣 石家庄看牛皮癣去哪个医院
- 2021-11-15银屑病是一种什么样的疾病?预防措施和控制应该注意以下几点
推荐阅读
- 石家庄治疗牛皮癣比较好的医院【评价靠谱】牛皮癣诊断
- 石家庄治疗牛皮癣医院排名 牛皮癣病因
- 牛皮癣症状 石家庄哪个银屑病医院比较好
- 石家庄看银屑病去什么医院比较好【疗效靠谱】
- 石家庄看银屑病什么医院比较好【名医汇聚】
- 石家庄哪家医院专业治牛皮癣 石家庄看牛皮癣去哪个医院
- 石家庄看银屑病去什么医院比较好【疗效靠谱】
- 石家庄哪家医院治疗牛皮癣比较好 石家庄比较好的牛皮癣医院
- 石家庄看银屑病哪家医院比较好【评价靠谱】
- 银屑病是一种什么样的疾病?预防措施和控制应该注意以下几点
- 者的蔬果问题
- 临床新知:关节病型银屑病的治疗困难重重
- 2011年进展和承诺:风湿病和麻风病领域研究热点
- 就是一个莲 让你长寿永不老(3)
- 皮肤过敏症状 皮肤过敏一般表现出的七大症状
- Science:合作型研究陷入挑战
- 预防银屑病住院的措施
- 患者的蔬果问题
- 塞尔基因银屑病药物Apremilast后期临床试验远超预期指标
- 银屑病的诊疗方法是什么
- 胃不好不能爱吃什么食物 这些食物一定不要碰
- 进食什么补白细胞 白细胞偏低进食它准没错
- 给退烧药是看体温还是看母亲的状态?解答你退烧的五个疑问
- 夏末来临预防扩散
- 患者烹饪禁区!
- 欧盟批准 LEO 制药银屑病有机体药物 Kyntheum
- 脓胞型银屑病确诊和治疗
- 养生花草茶 这样喝花草茶更肥胖症(15)
- 鲜为人知
- 用药问答:香烟患怎样调整药物剂量?
- 秋冬要到预防扩散
- 患者应多吃高蛋白营养
- 欧洲共同体批准 LEO 制药银屑病生物药物 Kyntheum
- 银屑病的诊断新方法是什么
- 养生花草茶 这样喝完花草茶更健康(15)
- 血清钙水平可预见甲氨蝶呤治疗银屑病效果
- 葛兰素史克的Xeljanz治疗性关节炎获得欧盟批准
- 秋冬来临防范扩散
- 患者的饮食简介
- 银屑病并发脂肪肝 无疑代谢合并症
- 脓胞型银屑病诊断和外科手术
- 如何去火 谨防去火的八大误区
- 小鼠钙水平可预测甲氨蝶呤治疗银屑病效果
- 艾伯维中止 Filgotinib 转而开发自有 JAK 抑制剂 ABT-494
- 预防银屑病罹患的措施
- 患饮食不作掉以轻心
- 乌司奴嘌呤—银屑病关节炎治疗的新生物制剂
- 银屑病的诊断原理